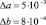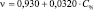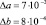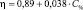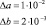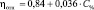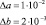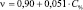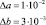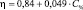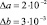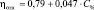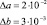К категории пищевых и биологически активных добавок относятся аминокислоты. Аминокислоты как основные составные части белков участвуют во всех жизненных процессах наряду с нуклеиновыми кислотами, углеводами и липидами. Схематично участие аминокислот в функционировании живого организма можно проиллюстрировать схемой (рис. 1). Препараты аминокислот широко представлены как в ассортименте пищевых и биологически активных добавок, так и в ассортименте лекарственных веществ. Комплексные препараты аминокислот, как правило, представлены в виде инфузионных растворов («Аминостерил», «Аминоплазмаль», «Инфезол», «Ликвамин» и т.д.) или сухих смесей для спортивного питания. Индивидуальные аминокислоты входят в состав таблеток («Глицин Форте», производство компании «Эвалар», «Клималанин» и т.д.), глазных капель («Тауфон»), растворов для инъекций («Тауфон», «Карнитен»), порошков («Левокарнитин», «Треонин», «Цистин» и т.д.).
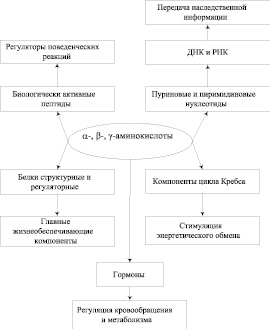
Рис. 1. Функции аминокислот в живом организме
При попадании в организм человека аминокислоты сразу же включаются в биохимические процессы [5]. Биохимический процесс, как любая химическая реакция, сопровождается изменением энергии системы, которой в данном случае и является человеческий организм. Если учесть тот факт, что человека называют «ходячим коллоидом» из-за высокого содержания воды в организме, то любая биохимическая реакция сопровождается изменением осмотической активности и вязкостных свойств биологических жидкостей [3, 4]. Поэтому исследование таких показателей, как вязкостные характеристики и коллигативные свойства растворов, содержащих аминокислоты, является крайне актуальным, поскольку позволяет выявить картину изменения того или иного показателя раствора от присутствия индивидуальной аминокислоты в различных концентрациях и картину изменения показателей раствора от присутствия смеси аминокислот. Поэтому целью данного исследования являлось изучение вязкостных характеристик водных растворов алифатических аминокислот линейного строения на примере глицина, β-аланина и ε-аминокапроновой кислоты.
Материалы и методы исследования
В качестве объекта исследования использовали водные растворы алифатических аминокислот глицина, β-аланина и ε-аминокапроновой кислоты. Определение вязкости термостатированных при 25°С растворов проводили при помощи вискозиметра ВПЖ-2, диаметр капилляра 0,73 мм, константа капилляра 0,03045.
Результаты исследования и их обсуждение
Рассмотрим функции алифатических аминокислот линейного строения – глицина, β-аланина и ε-аминокапроновой кислоты – в организме человека. Глицину принадлежит важнейшая роль в деятельности мозга, поскольку данная аминокислота участвует в образовании важнейших биологически активных соединений (пуриновых нуклеотидов, гема, креатина и др). Глицин выполняет функцию тормозного нейромедиатора, контролируя процессы формирования тонкой моторики пластических процессов и тонусных реакций поперечнополосатой мускулатуры. Поэтому в неврологической практике глицин широко используется для устранения повышенного мышечного тонуса [1]. В организме человека основная масса глицина сконцентрирована в спинном мозге. Глицин является регулятором обмена веществ, нормализует и активирует процессы защитного торможения в центральной нервной системе. Глицин обладает адреноблокирующим, антиоксидантным и антитоксическим действием, за счет чего уменьшает психоэмоциональное напряжение, агрессивность, конфликтность, улучшает настроение, повышает социальную адаптацию; повышает умственную работоспособность; облегчает засыпание и нормализует сон; уменьшает проявления вегетососудистых расстройств в целом и выраженность общемозговых расстройств при ишемическом инсульте и черепно-мозговых травмах; уменьшает токсическое действие алкоголя и других лекарственных средств, угнетающих функцию центральной нервной системы.
Аминокислота β-аланин, также, как и глицин, не является незаменимой, поскольку синтезируется в организме человека. β-Аланин участвует в синтезе пантотеновой кислоты (витамина В5), которая необходима для синтеза ацилкоэнзима А, который необходим для ферментов цикла карбоновых кислот (цикл Кребса) и жизненно необходим для синтеза основного субстрата энергетического метаболизма – аденозинтрифосфата АТФ. β-Аланин увеличивает уровень содержания пантотеновой кислоты и способствует стабилизации энергетического метаболизма, что важно для нормализации терморегуляции. β-Аланин является важнейшим координатором фонда возбуждающих и тормозных нейромедиаторов, повышает дыхательную активность нейроцитов, ускоряет утилизацию глюкозы и улучшает кровообращение. β-аланин широко используется в медицинской практике для лечения мигреней, цереброваскулярной недостаточности и других заболеваний нервной системы, связанных с нарушением кровообращения [1, 2, 5]. Данная аминокислота обладает выраженным диуретическим действием и при этом выгодно отличается от классических диуретических средств, так как не требует коррекции электролитов [1].
ε-аминокапроновая кислота не входит в перечень 20-ти аминокислот, из которых построены белки организма человека, но находит широкое применение в медицине и фармации, поскольку оказывает специфическое кровоостанавливающее действие при кровотечениях, способствует стабилизации фибрина и его отложению в сосудистом русле, способствует агрегации тромбоцитов и эритроцитов. Кроме этого ε-аминокапроновая кислота улучшает детоксикационную функцию печени и обладает противоаллергическим действием.
По результатам исследования вязкостных характеристик для глицина, β-аланина и ε-аминокапроновой кислоты наблюдается линейное увеличение кинематической, динамической и относительной вязкости с ростом концентрации аминокислот в индивидуальных растворах, а именно: для ε-аминокапроновой кислоты – до 6%, для β-аланина – до 20%, для глицина – до13,5% (рис. 2, 3).
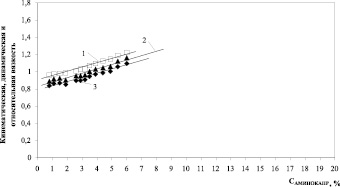
Рис. 2. Кинематическая (1), динамическая (2) и относительная (3) вязкость водных растворов ε-аминокапроновой кислоты
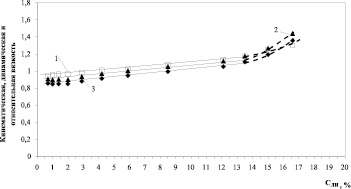
Рис. 3. Кинематическая (1), динамическая (2) и относительная (3) вязкость водных растворов глицина
Результаты линейной аппроксимации представлены в таблице. Для длинноцепочечной алифатической ε-аминокапроновой кислоты и для короткоцепочечной алифатической аминокислоты – β-аланина – линейность изменения характеристик вязкости зафиксирована практически до достижения предела растворимости в воде. Водные растворы глицина демонстрируют отклонения от линейности изменения характеристик вязкости, начиная с концентрации порядка 13% (рис. 3).
Коэффициенты уравнений линейной аппроксимации для кинематической, динамической и относительной вязкости аминокислот, ошибки определения коэффициентов и коэффициент корреляции
|
Аминокислота |
Кинематическая вязкость |
Динамическая вязкость |
Относительная вязкость |
|
Глицин |
R = 0,997
|
R = 0,993
|
|
|
β-аланин |
R = 0,996
|
R = 0,994
|
R = 0,994
|
|
ε-аминокапроновая кислота |
R = 0,983
|
R = 0,974
|
R = 0,974
|
Как было показано в [4] глицин, β-аланин и ε-аминокапроновая кислота, как алифатические аминокислоты, отличающиеся длиной углеводородной цепи и имеющие аминогруппу у последнего атома углерода, демонстрируют закономерное линейное изменение коллигативных свойств растворов с ростом концентрации. Наиболее осмотически активной является ε-аминокапроновая кислота, 1 моль/л которой увеличивает осмотическое давление раствора на величину порядка 3200 Па. Для глицина и ?-аланина этот показатель составляет соответственно 2750 Па и 3100 Па.
Анализ вязкостных характеристик водных растворов указанных аминокислот показывает, что и для них имеется тенденция линейного изменения кинематической, динамической и относительной вязкости с ростом концентрации аминокислот. Вместе с тем сохраняется тенденция по влиянию длины углеводородной цепи молекулы на характеристики растворов. Так ε-аминокапроновая кислота, как аминокислота, имеющая наиболее длинную углеводородную цепь, оказывает наиболее выраженное влияние на вязкость растворов – 1% ε-аминокапроновой кислоты увеличивает показатели кинематической, динамической и относительной вязкости на величину порядка 0,050 (данные по угловым коэффициентам линейных зависимостей характеристик вязкости приведены в таблице). Короткоцепочечные аминокислоты глицин и β-аланин имеют этот показатель на уровне 0,020 и 0,036 соответственно. Корреляционная связь между характеристиками вязкости и концентрацией веществ может быть оценена как сильная и достоверная, поскольку коэффициенты корреляции Пирсона по модулю входят в интервал [0,7; 1].
Выводы
1. Выявлены общие тенденции изменения некоторых характеристик водных растворов алифатических аминокислот линейного строения – глицина, β-аланина и ε-аминокапро- новой кислоты, имеющих концевую аминогруппу у последнего атома углерода. Общность проявляется в усилении влияния аминокислоты на вязкостные характеристики и на коллигативные свойства растворов с увеличением числа атомов углерода в цепи.
2. На примере указанного ряда аминокислот выявлена общая тенденция линейной корреляции вязкостных характеристик и коллигативных свойств водных растворов от концентрации веществ.
Библиографическая ссылка
Миняева О.А., Хисматуллина А.Р., Джафарова Т.Р., Тупкало Н.А., Якушева В.А., Пуховская К.С. ЗАКОНОМЕРНОСТИ ИЗМЕНЕНИЯ ВЯЗКОСТИ ВОДНЫХ РАСТВОРОВ НЕКОТОРЫХ АЛИФАТИЧЕСКИХ АМИНОКИСЛОТ // Рациональное питание, пищевые добавки и биостимуляторы. 2016. № 3. С. 22-26;URL: https://journal-nutrition.ru/ru/article/view?id=35756 (дата обращения: 11.04.2026).


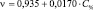
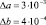
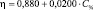
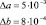
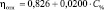 R = 0,994
R = 0,994